Sam é um astronauta que está na Lua há quase três anos e conta apenas com a companhia de GERTY, um robô capaz de tomar decisões autónomas em relação ao seu estado de saúde físico e mental, priorizando o seu bem-estar (parece bastante promissor, não acham?). O filme “Moon” traz-nos uma perspetiva um pouco menos catastrófica do que a do clássico de Stanley Kubrick “2001: Odisseia no espaço” e do seu robô HAL 9000, mas não foge completamente à receita criada por Hollywood – uma inteligência artificial que parece que nos vai resolver os problemas e que acaba por se virar contra nós. Os robôs GERTY e HAL 9000, que prestam um apoio essencial na monitorização do estado de saúde das pessoas e tomam decisões (médicas) autónomas, são apenas dois de muitos exemplos retirados da ficção e que têm contribuído para minar a nossa confiança em relação à Inteligência Artificial (IA).
A viagem que separa a ficção da realidade é longa e ainda pontuada por dúvidas. Que papel é que os robôs e sistemas de IA podem desempenhar na área da saúde? Desde as ferramentas de diagnóstico às de apoio à decisão, passando por planos de tratamento mais precisos ou terapias personalizadas, as respostas aos desafios médicos, vão-se multiplicando, em Portugal e no mundo.
Diagnósticos Precisos? A IA pode ajudar!
Um estudo da IDC, encomendado pela Microsoft, revelou que 79% das organizações de saúde já utilizam IA. Estima-se que, até 2025, haverá um aumento de 60% na adoção de soluções baseadas em IA pelos prestadores de cuidados de saúde. Um estudo da MedTech Europe, de 2020, indica que a utilização de IA nos cuidados de saúde poderia salvar cerca de 400 mil vidas anualmente e poupar aproximadamente 200 mil milhões de euros na Europa. Um estudo da Universidade da Califórnia em Los Angeles (UCLA) revelou que uma ferramenta de IA detetou cancro da próstata com uma precisão na ordem dos 84%, enquanto os médicos apresentaram uma taxa de 67%. A IA demonstrou alta sensibilidade em indicadores ignorados ou anotados incorretamente em radiografias de tórax. Ao olhar para estas estatísticas não é de estranhar que o INESC TEC esteja a trabalhar em múltiplas soluções onde a IA desempenha um papel crucial, como é o caso dos projetos europeus PHASE IV AI (diagnóstico, tratamento e gestão de dados em áreas críticas como o cancro), AI4Lungs (diagnóstico precoce e preciso de doenças pulmonares), LUCCA (identificação de padrões genéticos e moleculares associados ao cancro do pulmão), CINDERELLA (previsão dos resultados estéticos de cirurgias reconstrutivas em pacientes com cancro da mama) e do projeto CADPath.AI (um protótipo de IA que permite otimizar o diagnóstico de patologias colo-rectais). O objetivo? Promover diagnósticos e tratamentos mais precisos.
Mas quando falamos de IA aplicada à saúde esta deve ser explicável e ética. Quem é responsável quando um algoritmo falha? Como construímos a confiança entre médicos, pacientes e sistemas de IA? O uso de sistemas tendenciosos pode levar a decisões erradas ou perpetuar desigualdades?
Tiago Gonçalves, investigador do INESC TEC, começou a sua trajetória a trabalhar com inteligência IA na área da saúde, nomeadamente em projetos relacionados com análise de imagem médica, como é o caso do CINDERELLA. “Há 20 anos, a prioridade era curar a doença, e pouco se pensava no impacto estético. Hoje, especialmente no caso do cancro da mama, já existe essa preocupação. Portanto, este trabalho não se foca no diagnóstico ou no tratamento, mas na qualidade de vida das doentes após os procedimentos. O nosso objetivo é criar algoritmos que ajudem a avaliar se o resultado estético foi satisfatório, utilizando fotografias tiradas antes e depois da cirurgia”. Estamos a falar de algoritmos que analisam assimetrias, cicatrizes e outras alterações visíveis nas imagens.
Pensemos agora num algoritmo que não só classifica as imagens, como também apresenta um “mapa de saliência”, que destaca as zonas mais relevantes da imagem para a decisão da IA e acrescenta explicações textuais. A investigadora do INESC TEC Isabel Rio-Torto explica-nos tudo: “por exemplo, se um pulmão colapsou, faz sentido que o mapa mostre a área desse pulmão colapsado. Ou no caso de lesões de pele, será vantajoso que o mapa destaque zonas com bordas mais irregulares, algo que pode ser indicativo de cancro. Portanto, a ideia é termos um algoritmo que classifique imagens de raio-X, crie um mapa visual, e gere uma explicação em texto”. A vantagem? “Um artigo recente mostrou que os radiologistas preferem receber explicações textuais e visuais em conjunto. Mediram a diferença entre fornecer apenas mapas visuais, apenas explicações textuais, ou ambas, e concluíram que a combinação é a preferida”. Mas será esta explicação suficiente?
O combate ao viés e à falta de equidade: a qualidade dos dados importa
Para Tiago, a utilização da IA nas decisões críticas (high-stake decisions) exige um cuidado especial, pois trata-se de uma área em que uma decisão pode ter impacto direto na vida de uma pessoa, como é o caso da saúde. Apesar de os algoritmos serem cada vez mais precisos, é essencial testar as suas limitações e adaptá-los a diferentes realidades, já que os protocolos e contextos podem variar muito, por exemplo, de país para país. Algoritmos desenvolvidos na Europa podem não funcionar bem em África, devido às diferenças genéticas, culturais e socioeconómicas.
Um exemplo claro de viés é a diferença na precisão de sensores médicos em pessoas com diferentes tons de pele. “Os sensores de oximetria, por exemplo, funcionam melhor em pessoas de pele clara do que em pessoas de pele mais escura. Isso pode levar a diagnósticos tardios ou imprecisos, simplesmente porque os dados adquiridos não refletem a realidade dessas populações. Ou seja, o problema começa na recolha de dados e afeta todo o processo”, explica o investigador.
No que diz respeito à equidade (fairness) na IA, Tiago Gonçalves adianta que é possível ajustar os algoritmos para evitar discriminações. “Os algoritmos têm tendência a beneficiar casos mais comuns, porque a maioria dos dados disponíveis reflete essa realidade. Mas podemos incorporar mecanismos que reconheçam quando um caso é menos comum e ajustem as decisões para garantir maior precisão”.
Isabel acrescenta que um dos prolemas da aplicação da IA em contextos clínicos é o facto de, na maioria dos casos, os algoritmos serem treinados com dados de apenas um hospital. E quando transitamos o mesmo algoritmo para outro hospital? “Para as mesmas doenças, os resultados podem não ser tão bons. Basta mudar o equipamento que tirou a radiografia ou as condições de luz, e isso pode afetar o desempenho do modelo. Este é um problema que ainda não está completamente resolvido”.

Efetivamente, trabalhar com dados de qualidade pode evitar enviesamentos. “Os algoritmos aprendem com os dados que recebem. Se forem treinados com relatórios de médicos que cometem erros ou têm práticas enviesadas, é isso que vão reproduzir. É o famoso ‘entra lixo, sai lixo’”, refere Isabel Rio-Torto, mencionando o caso do sistema COMPAS (Correctional Offender Management Profiling for Alternative Sanctions) usado nos tribunais dos Estados Unidos, que demonstrou enviesamento contra a população negra porque os dados com que foi treinado já refletiam essa desigualdade. “Os algoritmos dependem totalmente dos dados com que são treinados. Se os dados tiverem ruído, erros ou vieses, os algoritmos irão aprender isso também. Por exemplo, no caso de doenças raras, onde há menos dados disponíveis, os algoritmos podem não ser tão eficazes”, acrescenta Tiago.
Explicabilidade e aprendizagem federada
O crescimento da IA explicável e interpretável foi, segundo Tiago Gonçalves, impulsionado por estas questões éticas. A motivação por detrás de muitos avanços na IA explicável é garantir que os sistemas sejam justos e transparentes, especialmente em áreas como saúde.
Mas Isabel fala da dificuldade em algoritmos explicáveis e garantir que os modelos são, de facto, interpretáveis. “Há técnicas que permitem gerar explicações a posteriori, mas outros colegas e eu somos céticos quanto a essas abordagens. Não temos garantias de que essas explicações correspondem ao que o modelo realmente está a fazer. A única forma de garantir interpretabilidade é construir o modelo com explicabilidade integrada desde o início”.
Há um longo caminho a percorrer para garantir que essas soluções sejam eficazes. O AI ACT da União Europeia é um primeiro passo, mas para Tiago é essencial regulamentações claras que definam padrões para o desenvolvimento e aplicação da IA na saúde. “Os algoritmos precisam ser monitorizados continuamente, porque a realidade muda. Um algoritmo que funcionava há 10 anos pode já não ser adequado hoje”. Uma das soluções que está a ser explorada é a aprendizagem federada (Federated Learning), uma abordagem que permite treinar modelos de forma colaborativa sem a necessidade de centralizar os dados, preservando a privacidade dos dados. “Cada hospital mantém os seus dados localmente, mas contribui para a construção de um modelo global mais robusto”, clarifica o investigador.
Há algo em que Tiago e Isabel estão plenamente de acordo: a IA deve ser sempre encarada como uma ferramenta de apoio, e não como substituta dos profissionais. “A decisão final deve ser sempre humana. Por exemplo, os radiologistas já admitiram que a IA é muito útil para filtrar os casos mais simples, para que possam focar-se nos mais complexos. Portanto, a IA é uma aliada, não uma ameaça”, avança Tiago. Isabel acrescenta que dificilmente a IA irá fazer o trabalho de um médico, mas é essencial que estes compreendam as suas potencialidades: “a decisão final deve continuar a ser do médico. Penso que, talvez, as novas gerações de médicos, que já estão mais habituadas às tecnologias, venham a adotar estas ferramentas com mais facilidade, sobretudo se as mesmas forem introduzidas durante a formação. Por um lado, podem ajudar os médicos a compreender melhor como os algoritmos funcionam e, por outro, apoiar a própria formação dos médicos”.
Aqui entra também a necessidade da colaboração entre diferentes áreas de conhecimento. “Os investigadores precisam de ter consciência do impacto do que estão a desenvolver, e os profissionais da saúde, do direito e da política também precisam de compreender as limitações e potencialidades da IA. Só com essa colaboração multidisciplinar poderemos garantir que a tecnologia sirva, de facto, para melhorar a vida das pessoas”, conclui Tiago.
O sucesso dos modelos de IA no diagnóstico e tratamento da epilepsia
Sabiam que a IA pode prever crises epiléticas com uma precisão de até 99%? Vamos falar de casos reais, onde a colaboração multidisciplinar já dá frutos. No Serviço de Neurologia do Centro Hospitalar Universitário São João (CHUSJ), pretende-se utilizar uma ferramenta de apoio à decisão clínica para ajudar os médicos em casos de epilepsia refratária (, ou seja, aqueles cujas crises epiléticas não são controladas com medicamentos), nomeadamente na interpretação de sinais cerebrais. José Almeida é o investigador do INESC TEC que está a desenvolver este método de identificação das zonas epileptogénicas através do uso de machine learning. “A partir de gravações de sinais de eletroencefalograma (EEG) intracerebral, são extraídas características como a conectividade entre diferentes canais, e aplicados algoritmos para classificar as áreas do cérebro que geram as crises. Portanto, trata-se de um software que faz uso de diferentes sinais e imagens cerebrais adquiridas durante e entre crises e que por isso apresenta elevada sensibilidade”, adianta.
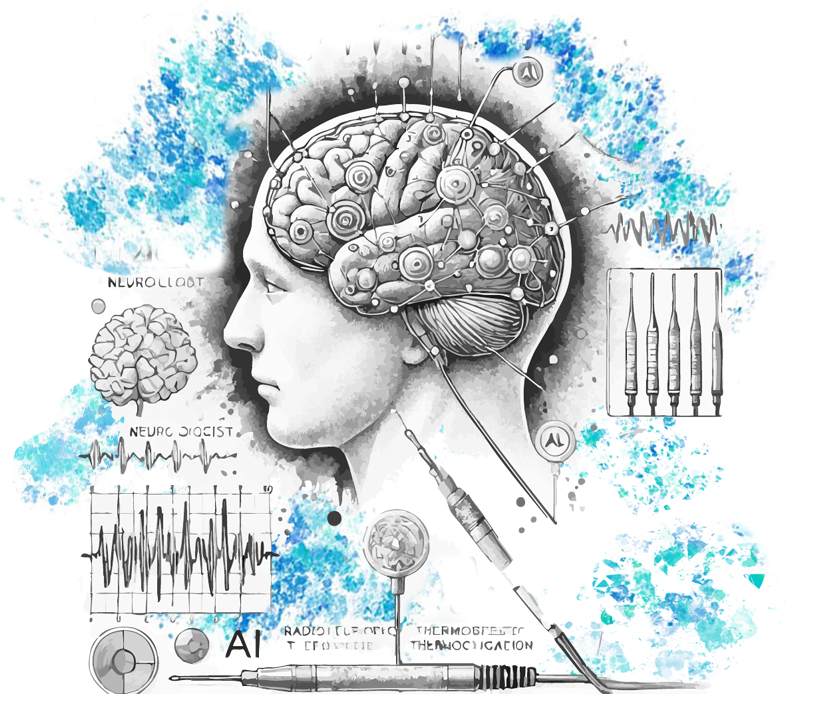
Mas José quer ir ainda mais longe e, está agora a trabalhar num protocolo que permita aos neurocirurgiões usar as informações extraídas pelos algoritmos para definir um tratamento. Falamos de uma técnica designada por termocoagulação que utiliza os elétrodos intracranianos do EEG para emitir impulsos de radiofrequência e, dessa forma, aumentar a temperatura nas áreas selecionadas. O aumento da temperatura provoca a termocoagulação, ou seja, queima o tecido na região-alvo, com o objetivo de reduzir ou eliminar as crises epiléticas. “O que torna esta investigação inovadora é a proposta de criar um protocolo que ajude os neurocirurgiões a aplicar a lesão de forma mais precisa, minimizando os efeitos secundários e melhorando os resultados do tratamento. Atualmente, essa decisão é feita apenas por avaliação visual, o que pode ser subjetivo e levar a erros, especialmente em equipas menos experientes”, explica o investigador. Além de desenvolver o protocolo para a aplicação da termocoagulação, o grupo de investigação pretende criar ferramentas que ajudem a avaliar a eficácia do procedimento.
José Almeida ressalva que, embora a termocoagulação seja um procedimento relativamente acessível, seguro e simples de ser implementado – exigindo apenas os elétrodos e uma máquina de radiofrequência –, ainda há muitos desafios, como a articulação com os hospitais para obter dados de pacientes e a análise dos sinais cerebrais, que têm amplitude muito baixa.
Um dos próximos passos é combinar essas ferramentas com outras tecnologias para aplicações mais amplas. “Há a possibilidade de criar dispositivos implantáveis que respondam a estímulos específicos baseados em biomarcadores, como os utilizados em estimulação cerebral profunda (DBS). A tecnologia também pode ser adaptada para tratar outras doenças”, revela.
No mundo real, estamos a trabalhar em soluções que primam pela colaboração entre profissionais de saúde e investigadores e que procuram usar a IA de forma ética. Portanto, não se preocupem; ainda estamos longe encontrar o robô GERTY na próxima consulta. Mas…até quando?


 Notícias, atualidade, curiosidades e muito mais sobre o INESC TEC e a sua comunidade!
Notícias, atualidade, curiosidades e muito mais sobre o INESC TEC e a sua comunidade!